Kemija
Jesenski rok 2010.
U sljedećim zadacima dopunite tablice ili rečenice upisivanjem pojmova koji nedostaju.
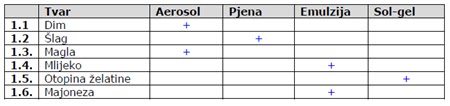
1. Nabrojene tvari razvrstajte na vrste koloidnih otopina: aerosol, pjena, emulzija i sol-gel. Obilježite znakom X vrstu koloidnih otopina kojoj pripada pojedina tvar.
Točni odgovori:
2. a) Napišite odgovarajuće kemijske formule navedenih spojeva.
2.1. aluminijev sulfid ____________________
2.2. kalcijev perklorat ____________________
2.3. amonijev hidrogensulfat ____________________
Točni odgovori:
2.1. Aluminijev sulfid Al2S3
2.2. Kalcijev perklorat Ca(ClO4)2
2.3. Amonijev hidrogensulfat NH4HSO4
2. b) Napišite odgovarajuće kemijske nazive navedenih spojeva.
2.4. Ca(CN)2 _____________________________________
2.5. FePO4 ∙ 2 H2O _____________________________________
2.6. KNO2 _____________________________________
Točni odgovori:
2.4. Ca(CN)2 kalcijev cijanid
2.5. FePO4 ∙ 2H2O željezov(III) fosfat dihidrat
2.6. KNO2 kalijev nitrit
3.1. Poredajte po veličini od najmanje do najveće ove jedinke: Ar, K+, Cl−, Ca2+, S2−.
______________________________________________________________
3.2. Što je zajedničko jedinkama iz zadatka 3.1.?
______________________________________________________________
3.3. Napišite elektronsku konfiguraciju osnovnoga stanja atoma sumpora.
______________________________________________________________
3.4. Nacrtajte Lewisove simbole kloridnoga iona, atoma argona i kalijeva kationa.
Točni odgovori:
3.1. Ca2+, K+, Ar, Cl−, S2− (ili obrnutim redom)
3.2. Elektronska konfiguracija, ukupan broj elektrona ili to su izoelektronske čestice
3.3. 1s2 2s2 2p6 3s2 3p4
3.4.
4. Kao elementarna tvar kalcij nema značajnije uporabe, no kalcijevi spojevi poput krede, gipsa, vapnenca i mramora su vrlo učestali i rabljeni u svakodnevnome životu.
Hidroksiapatit, Ca5(PO4)3(OH), temeljni je sastojak naših kostiju i zuba. Elementarni kalcij prvi je izolirao engleski kemičar Humphrey Davy 1808. godine propustivši istosmjernu električnu struju kroz taljevinu kalcijeva klorida.
Kristali kalcija pripadaju kubičnomu sustavu, a njegova elementarna ćelija je kocka s duljinom stranice od 5,56 ∙ 10−8 cm. Gustoća kalcija je 1,55 g cm−3.
Izračunajte broj atoma u elementarnoj ćeliji kristala kalcija i odredite kojoj vrsti atomskih slagalina pripada.
Postupak:
Broj atoma ___________
Slagalina _________________________________________________________
Točni odgovori:
Račun:
V(kocke) = a3 = (5,56∙10−8 cm)3 = 1,719 ∙ 10−22 cm3
mkocke = 2,664 ∙ 10−22 g
ma(Ca) = 6,655 ∙ 10−23 g
mkocke/matoma = 4
Elementarna ćelija sadrži 4 atoma kalcija, stoga je to plošno centrirana kocka.
5. Kristale jedne soli izgrađuju kalcijevi ioni i njima izoelektronski jednoatomni, dvovalentni anioni.
5.1. Napišite kemijsku formulu te soli kalcija.
______________________________________________________________
5.2. Kristalna struktura kalcijeve soli iz zadatka 5.1. pripada tipu struktura natrijeva klorida. Izračunajte gustoću te kalcijeve soli i iskažite je jedinicom g mL–1 ako je duljina brida elementarne (jedinične) ćelije 0,5690 nm.
Postupak:
Rezultat: ________________________
5.3. Koliki je koordinacijski broj kationa i aniona u kristalu tvari iz zadatka 5.1. s obzirom na tip kristalne strukture?
______________________________________________________________
5.4. Iz jednoga grama taljevine kalcijeva spoja iz zadatka 5.1. elektrolizom je izlučen sav prisutan kalcij. Izračunajte naboj potreban za taj pokus. Pretpostavite da je iskorištenje struje bilo potpuno (100%-tno).
Postupak:
Rezultat: ________________________
Točni odgovori:
5.1. CaS
5.2.
Račun:
m(CaS) = 1,198 ∙ 10−25 kg
m(ćelije) = 4,791 ∙ 10−25 kg
V = 1,842 ∙ 10−28 m3
ρ(CaS) = 2,60 g mL−1
Rezultat: ρ(CaS) = 2,60 g mL−1
5.3. N(kation) = N(anion) = 6
5.4. Rješenje:
Ca2+(l) + 2 e− → Ca(s)
Q = n(e−) · F
Q = n(Ca2+) · F
Q = m(CaS)/M(CaS) · z · F
Q = (1 g/72,14 g mol−1) · 2 · 6,02 · 1023 mol−1· 1,60 · 10−19 C = 2670 C